CMV HHV6,7,8 R-gene®
Kit de PCR en tiempo real para la detección y cuantificación de CMV, HHV -6, y la identificación de ADN de HHV-7 y HHV-8
- Una cuantificación precisa de carga viral de CMV y HHV-6 con una amplio rango lineal
- Detección cualitativa de HHV-7 y HHV-8
- Kit listo para su uso incluyendo control interno y estándares de cuantificación para CMV y HHV-6
- Validado CE-IVD para todas las principales plataformas de extracción y PCR en tiempo real
Necesita más información
Ventajas de CMV HHV6,7,8 R-gene®
El CMV, HHV-6, HHV-7, HHV-8 son responsables de una amplia gama de patologías. Por eso es importante lograr una detección y monitorización optimizada de la infección por CMV, HHV-6, HHV-7 y HHV-8. CMV HHV6,7,8 R-gene® es una solución ideal, que ofrece una detección rápida y específica. Puede detectar la infección antes de que los síntomas clínicos aparezcan, mejorando las opciones de manejo de pacientes, realizando pruebas durante el tratamiento para medir la efectividad del mismo, y realizándolas después para controlar posibles recaídas. Además - para mayor integralidad - puede usarse con muchos de los kits de la gama R-gene®, que le permite identificar y/o cuantificar varios virus en la misma una muestra a la vez, o analizar varias muestras distintas en la misma serie.
- Sensible y reproducible
- Medida fiable de CMV y HHV6; identificación de infección por HHV-7, HHV-8
- Amplio rango lineal para carga vírica de CMV y HHV-6
- Estandarizado
- Perfiles de pruebas armonizados para realizar múltiples ensayos a la vez
- Procesado uniforme con la gama de productos R-gene® (CMV R-gene®, HSV1 HSV2 VZV R-gene®, BK Virus R-gene®, Adenovirus R-gene®, EBV R-gene®, PARVOVIRUS B19 R-gene®)
- Flexible
- Validado para su uso con múltiples tipos de muestras
- Prepare muestras manualmente o utilice la preparación automatizada con NUCLISENS® easyMAG®, NUCLISENS®EMAG® y la plataforma de preparación de ensayos ESTREAM®
- Validado para las principales plataformas PCR en tiempo real
*proximamente
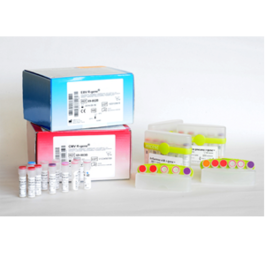
Kit completo con todo lo que necesita
El ensayo CMV HHV6,7,8 R-gene® es un kit de detección molecular listo para su uso. Utilizar PCR en tiempo real tras la extracción del ADN vírico, mide la carga viral del CMV y HHV-6, y permite la detección de HHV-7 y HHV-8. Funciona amplificando y detectando simultáneamente regiones específicas de los genomas de CMV, HHV-6, HHV-7 y HHV-8, utilizando la tecnología Taqman nucleasa- 5'.
- Cuatro estándares de validación garantizan una medida precisa de la carga viral de CMV y HHV-6
- El control de sensibilidad valida el rendimiento del ensayo
- El control interno (IC2) comprueba el proceso de extracción, incluyendo la lisis y la presencia de inhibidores de amplificación en la muestra
- Incluye todos los reactivos necesarios optimizados para cuantificar CMV (90 tests) y HHV-6 (30 tests) y detectar HHV-7 (10 tests) y HHV-8 (10 tests). Para uso en diagnóstico in vitro.
- Reactivos adicionales: aumente su número de tests con la master mix de PCR para HHV6 r-gene® (69-100R6 – 60 tests), HHV7 r-gene® (69-100R7 - 20 tests), y HHV8 r-gene® (69-100R8 - 20 tests).
Procedimiento sencillo
El kit CMV HHV6,7,8 R-gene® es fácil de usar. Sólo hace falta añadir la muestra de ADN extraída a la master mix de PCR lista para su uso y empezar la reacción de PCR en tiempo real, siguiendo un programa de ciclado optimizado descrito en las "Instrucciones de uso".

BIOMERIEUX, el logo azul, ARGENE®, R-GENE®, EASYMAG® y NUCLISENS®, se emplean, dependen y/o son marcas registradas pertenecientes a bioMérieux S.A. o a cualquiera de sus filiales o de sus empresas.
Cualquier otro nombre o marca registrada es propiedad de su respectivo propietario.
|
Especificaciones técnicas - CMV HHV6,7,8 R-gene® (69-100B |
|
|---|---|
|
Principio de la prueba |
Detección genómica y cuantificación de CMV y HHV-6. Detección genómica de HHV-7 y HHV-8 |
|
Información de pedido |
Referencia 69-100B: Kit de detección y cuantificación CMV HHV6,7,8 R-gene® |
|
Tecnología |
PCR en tiempo real / Tecnología Taqman nucleasa-5' |
|
Diana génica |
CMV: gen para la codificación de la proteína ppUL83 |
|
Espécimen* |
Sangre total, plasma, LCR, líquido amniótico, suero, orina, BAL, biopsias |
|
Límite de detección |
CMV: LoD 95%: 446 Copias/ mL de muestra de sangre total |
|
Rango lineal de cuantificación |
CMV en muestra de sangre total: 9,43 log (Cp/mL) a 2,63 log Cp/mL) |
|
Controles incluidos |
Extracción + Control de inhibición, control de sensibilidad, control negativo |
|
Resultados en |
75 minutos (paso de extracción no incluído) |
|
Unidad de comunicación |
Copias/mL |
|
Número de tests |
140 tests |
|
Condiciones de almacenamiento |
-18°C/-22°C |
|
Plataformas de extracción validadas* Manual / Automatizada |
QIAamp DNA Blood Mini kit |
|
Plataformas validadas de amplificación* |
Life Technologies (Applied Biosystems) |
|
Estado |
Para uso en diagnóstico in vitro, marcado CE en Europa |
* por favor consulte
Datos rápidos sobre virus CMV, HHV-6, HHV-7 y HHV-8
¿Qué son CMV, HHV-6, HHV-7, HHV-8?
Cytomegalovirus (CMV), herpesevirus-6 humano (HHV-6), herpesevirus-7 humano (HHV-7) y herpesevirus-8 humano (HHV-8) son virus caracterizados por una alta seroprevalencia (que va del 50% al 100%, dependiendo de la región geográfica) y que son responsables de una amplia gama de patologías. La infección primaria sucede por lo general en la infancia. La diseminación vírica en sangre puede dar lugar a signos clínicos benignos y raros. CMV, HHV-6, HHV-7 y HHV-8 establecen una infección latente a lo largo de la vida. No obstante, los virus suelen reactivarse en caso de una inmunosupresión.
¿Quién tiene mayores riesgos?
La gravedad de la infección depende del estado inmune del huésped (p.ej., pacientes con SIDA y pacientes con órganos trasplantados suelen ser considerados huéspedes débiles). CMV está asociado con enfermedades neurológicas y neumopatías. En casos severos, puede dar lugar a mortalidad en pacientes inmunocomprometidos. HHV-6 y HHV-7 también son muy proclives a infecciones oportunistas en pacientes inmunocomprometidos. HHV-6 y HHV-7 suelen aumentar las infecciones secundarias por CMV a través de un proceso de reactivación cruzada. Cuando se da una infección primaria, HHV-6 también es la posible causa de síndromes mononucleósicos, linfoadenopatías y hepatitis. HHV-8 se asocia con enfermedades linfoproliferativas como el sarcoma de Kaposi, la enfermedad de Castleman y algunos linfomas.
¿Cuáles son los beneficios de las pruebas de CMV, HHV-6, HHV-7, HHV-8?
Los ensayos basados en PCR en tiempo real para CMV, HHV-6, HHV-7 y HHV-8 permiten una detección rápida y específica antes de que los síntomas clínicos aparezcan, para ayudar a mejorar el manejo del paciente, que resulta especialmente importante para pacientes inmunocomprometidos. Las pruebas ayudan a seguir la efectividad de un tratamiento activo y pueden usarse para monitorizar una recaída tras el tratamiento.
CMV HHV6,7,8 R-GENE®: PUBLICACIONES
-
Updated international consensus guidelines on the management of cytomegalovirus in solid-organ transplantation.
Kotton CN, Kumar D, Caliendo AM, Asberg A, Chou S, Danziger-Isakov L, Humar A; Transplantation Society International CMV Consensus Group.
Transplantation. 2013 Aug 27;96(4):333-60 -
Xavier Roblin, Sylvie Pillet, Abderrahim Oussalah, Philippe Berthelot, Emilie Del Tedesco, Jean-Marc Phellip, Marie-Laure Chambonnière, Olivier Garrau, Laurent Peyrin-Biroulet and Bruno Pozzetto.
Am J Gastroenterol. 2011 Nov;106(11):2001-8 -
C.Rodier-Bonifas, P.-L Cornut, G.Billaud, B.Lina, C.Burillon, P.Denis.
Journal Français d'ophtalmologie 2011 34, 24-29 -
J.Bordes, J.Maslin, B.Prunet, E.d'Aranda, G.Lacroix, P.Goutorbe, E.Dantzer, E.Meaudre.
Burms (2011), doi:10.1016/j.burns.2010.11.006. -
Birgit D.A. Michelin, Ita Hadzisejdic, Michael Bozic, Maja Grahovac, Markus Hess, Blazenka Grahovac, Egon Marth, Harald H. Kessler.
J.Clin. Microbiol., February 2008. -
Deback C, Agbalika F, Scieux C, Marcelin AG, Gautheret-Dejean A, Cherot J, Hermet L, Roger O, Agut H.
J Virol Methods. 2008 May;149(2):285-91. Epub 2008 Mar 10. -
Claire Deback, M.D.; Felix Agbalika; Catherine Scieux; Anne-Geneviève Marcelin; Agnès Gautheret-Dejean; Janine Cherot; Laurence Hermet; Odile Roger; Henri Agut.
J Virol Methods May 2008:149(2):285-91. -
Aurélie Ducroux, Samira Cherid, Alexandra Benachi, Yves Ville, and Marianne Leruez-Ville.
J of Clinical Microbiology. June 2008,p.2078-2080. -
C.Deack, A.M Fillet, N. Dehdin, B. Barrou, S. Vamous, F. Najoullah, F. Bricaire, H. Agut.
J. of Clinical Virology 40 (2007) 173-179. -
Multicentric evaluation of a new commercial cytomegalovirus real-time PCR quantitation assay.
Gouarin S, Vabret A, Scieux C, Agbalika F, Cherot J, Mengelle C, Deback C, Petitjean J, Dina J, Freymuth F.
J Virol Methods.2007 dec;146(1-2):147-54
Posters :
-
bioMérieux Argene Range verifications on the ViiA7 (Fast and Standard Blocks) and ABi 7500 Fast Dx Real Time PCR Platforms
Magro Stephane; Delarivière Audrey; Berriot Aurelie; Turc Amelie; Moiroud Elise; Derome Andrew; Alberti-Segui Cristina; Grosz Sophie; Vidal Celine; Poyet-Gelas Fanny and Barranger Come
ESCV 2014, Prague -
Marie Gueudin, Alexandre Louvel, Jean-Christophe Plantier
Laboratoire de virologie, CHU de Rouen, Université de Rouen, France
ECV 2013
-
Sylvie Pillet et al
Virology Unit, University Hospital of Saint-Etienne
ECV 2013
-
Sylvie Pillet et al
Virology Unit, University Hospital of Saint-Etienne
ECV 2013
-
Improvement of NUCLISENS® EASYMAG® whole blood extraction protocol for virus
Vignoles et al.
CVS 2013
-
Vignoles et al.
ESCV 2011 -
Vignoles M. ; Barranger N. ; Bertrand M. ; Raoux N. ; Magro S. ; Barranger C. ; Joannes M.
Poster 14th annual meeting of th eeuropean society for clinical virology, Madeira, 2011 -
Alain et al.
French National reference center for Cytomegaloviruses, CHU Dupuytren, Limoges France
CMV Workshop Nuremberg 2011 -
Alain S. ; Boyer B. ; Vignoles M. ; Joannes M. ; Barranger C. ; Ploy M-C.
CMV Workshop Nüremberg 2011.
-
Germi et al.
Unit of Virus Host Cell Interactions, Grenoble
ESCV 2011
-
Laboratory of Virology, Nancy University Hospital, France
CVS 2010
-
Colak et al.
Akdeniz university, School of Medicine, Antalya.
ESCV 2009 -
Mutlu et al.
University School of Medicine Medical Microbiology Department, Antalya, Turkey.
ESCV 2009
-
HHV6 encephalitis in immunocompetent patients, is it a myth ?
Rozé et al.
Département de Microbiologie, Centre Hospitalier Universitaire de Brest
CVS 2009
-
Pillet et al.
Laboratoire de Bacteriologie-Virologie-Hygiène, Hopital Nord, CHU de Saint-Etienne, France.
ECCMID 2008 -
Performance Evaluation of the Argene Biosoft CMV HHV-6, 7, 8, R-gene Assay
Zhang et al.
North Shore LIJ Health System Laboratories, Lake Success, NY
CVS 2007